2026年1月23日,日本大阪大学的的研究团队在国际期刊《Nature Communications》发表了题为《Endothelial stem cells of the retinal vasculature reside in the optic nerve》(即《视网膜血管内皮干细胞存在于视神经中》)的重磅研究成果。
之所以值得专门分享这篇文献,是因为它颠覆了视网膜血管再生依赖自身内皮细胞的传统认知,首次证实视神经是视网膜血管内皮干细胞的关键储存库,兼具基础科学突破与临床转化价值,极具分享意义。
从基础研究层面,它填补了视网膜血管内皮祖细胞来源的核心空白,揭示了视神经作为干细胞生态位的全新功能,改写了眼部血管生物学的理论框架。研究明确了内皮干细胞的层级分化规律与VEGF、Notch等关键调控通路,为理解视网膜血管稳态维持、损伤修复机制提供了全新视角,也为中枢神经系统血管再生研究提供了重要参考。
从临床应用层面,该发现为糖尿病视网膜病变、视网膜静脉阻塞等缺血性致盲眼病带来全新治疗方向。靶向激活或移植视神经内皮干细胞,可实现生理性血管修复,突破现有抗VEGF治疗仅抑制病理性新生血管的局限;同时,基于干细胞微环境的药物研发,有望开发出微创、高效的内源性修复疗法。
此外,研究挑战了组织特异性干细胞定位的传统教条,推动再生医学范式革新,其技术方法与研究思路也为其他器官干细胞研究提供了借鉴。无论是科研工作者、临床医生,还是关注眼底病治疗的从业者,都能从中获得全新思路,因此值得广泛传播与深入研读。
以下为全文分享:
一、摘要
视网膜细胞(尤其是感光细胞)代谢活跃、能量需求极高,因此通过视网膜血管有效输送氧气和营养物质是维持视网膜功能的关键。视网膜血供紊乱(尤其是长期紊乱)可导致视力丧失。血管内皮细胞作为血管内壁的主要构成细胞,在包括眼后部感光视网膜在内的多种组织中,对维持健康血液循环至关重要。然而,血管内皮细胞如何维持视网膜功能(并助力损伤修复)的机制尚不明确。本研究通过单细胞RNA测序、集落形成实验和谱系示踪分析,发现并证实了一种新的调控系统:视网膜血管内皮细胞由视神经中的干细胞/祖细胞库持续供给。
二、引言
成体干细胞的协同活动是维持组织稳态的核心,尤其在高更新率的组织中。事实上,在上皮、造血、血管和神经系统中,干细胞系统会在不同时间点、以不同速度响应各类慢性内外应激,完成稳态重塑。急性损伤时,干细胞被激活并启动组织修复;若干细胞系统功能失调,组织重塑失败则必然引发疾病。
不同组织来源的内皮细胞具有独特的转录谱,单细胞RNA测序(scRNA-seq)已证实其常聚集成器官特异性亚型。部分研究提示,驻留型内皮干细胞是血管修复与更新的基础,但血管内皮祖细胞是否存在仍存在争议。
视网膜作为眼球最内层的感光组织,是视觉形成的关键。由于视网膜细胞的能量消耗甚至超过大脑,血供中断导致的氧和营养供应受限会严重损害视力。事实上,缺血性视网膜病变(如糖尿病视网膜病变、早产儿视网膜病变、视网膜静脉阻塞)是视力丧失的主要原因。除供氧和营养外,视网膜血管还在调控免疫细胞迁移、维持组织稳态中发挥关键作用。内皮细胞作为视网膜血管内壁的构成者,对维持组织稳态和血管新生(从现有血管生成新血管的过程)至关重要。本研究发现,视神经中存在大量视网膜血管内皮干细胞(VESCs),它们不仅在稳态条件下为视网膜供给内皮细胞,还在血管损伤后被快速募集,参与受损血管的修复。
三、结果
3.1视神经中的内皮干细胞
在小鼠眼中,眼动脉穿过眶部向眼球巩膜部延伸,视网膜中央静脉则更靠近视神经。如既往研究所述,视网膜和视神经平铺标本的PECAM1(CD31,泛内皮标志物)染色显示,视网膜中央静脉沿视神经嵌入视网膜。为探究视网膜内皮干细胞/祖细胞,本研究首先聚焦于内皮祖细胞标志物CD157和CD201。为验证视网膜血管中是否存在内皮祖细胞,分选了CD45阴性CD31阳性的内皮细胞。结果显示,视网膜中约1%–2%的细胞为CD157阳性,比例远低于其他器官中约5%的水平。进一步分析发现,视网膜血管和视神经来源的CD157阳性或CD201阳性细胞比例超过5%,而视神经本身则含有超过20%的CD157阳性或CD201阳性内皮祖细胞,视网膜中央静脉中也存在CD157阳性或CD201阳性细胞。
对比视网膜和视神经内皮细胞的克隆扩增能力,成年小鼠CD45阴性CD31阳性细胞的集落形成实验显示,视神经来源的内皮细胞可产生更多内皮细胞。此外,同时表达CD157和CD201的细胞表现出内皮集落形成细胞的特征,而CD157阳性CD201阴性、CD157阴性CD201阳性及CD157阴性CD201阴性细胞则无此特性。
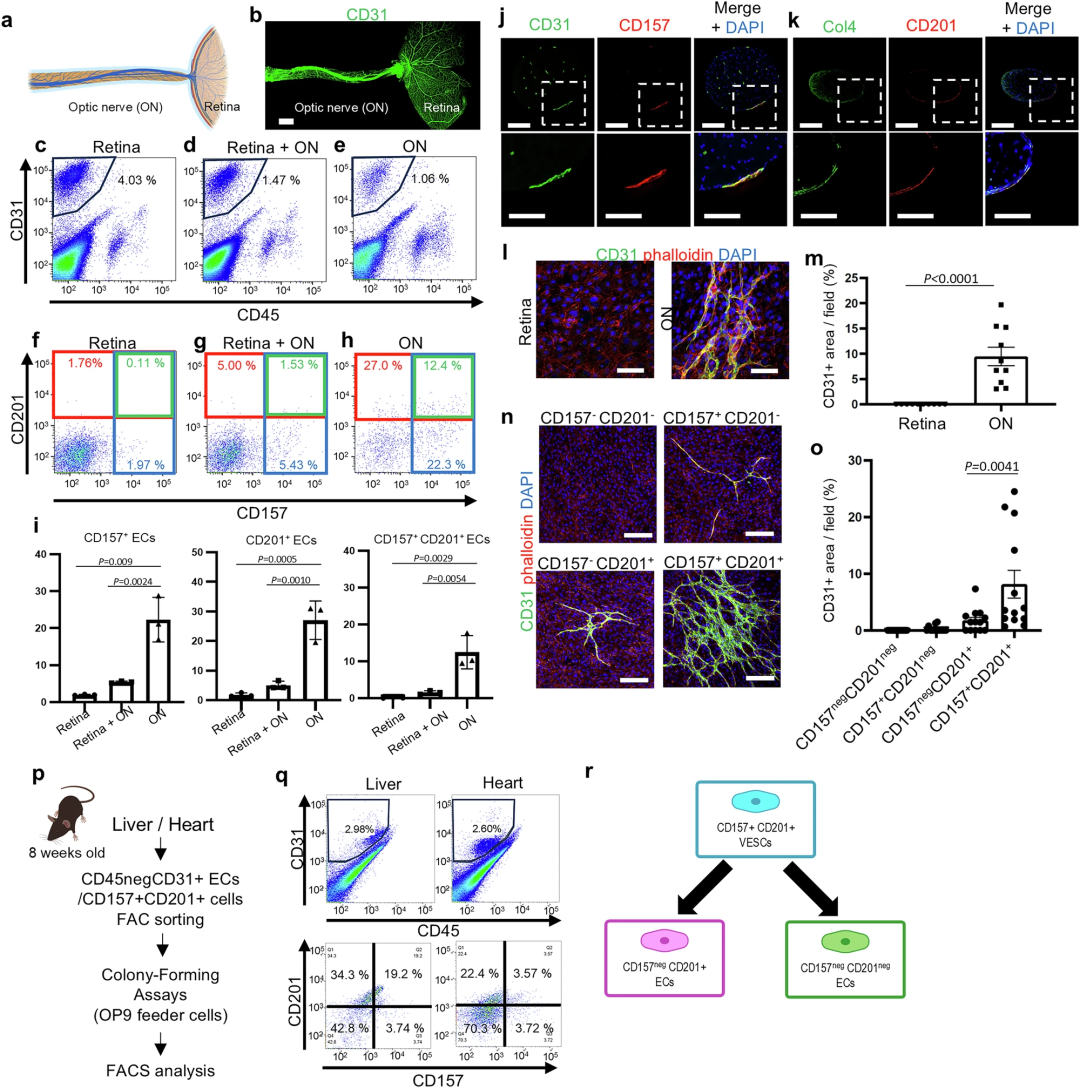
图1:视神经血管中富含内皮干细胞/祖细胞标志物阳性细胞
为明确血管内皮干细胞(VESCs)下游的细胞层级,通过荧光激活细胞分选(FACS)重新分析了CD157阳性CD201阳性内皮细胞来源的内皮集落形成细胞。由于视神经中可获取的内皮细胞数量不足,本研究选用肝脏和心脏(其集落形成能力良好,且CD157阳性CD201阳性VESCs的比例与视网膜+视神经相近)进行分析。结果显示,CD157阳性CD201阴性细胞占集落的比例不足5%,CD157阴性CD201阳性细胞占20%–30%,CD157阴性CD201阴性细胞占40%–70%。这提示存在层级结构:CD157阳性CD201阳性VESCs位于上游,CD157阴性CD201阳性内皮细胞和CD157阴性CD201阴性内皮细胞位于下游。
3.2稳态条件下视网膜血管内皮细胞存在于视神经中
对8周龄小鼠分选的视网膜内皮细胞(CD45阴性CD31阳性)进行3'和5'端scRNA-seq分析,共纳入44,358个“仅视网膜”和“视网膜+视神经”来源的内皮细胞,鉴定出多个内皮细胞簇,其中混杂少量感光细胞、Müller细胞、双极细胞和单核细胞。在内皮细胞群中,检测到表达Bst1(CD157)和Procr(CD201)的独特细胞簇,且位于细胞分化的上游,推测为VESCs亚群。高表达Bst1的亚群同时表达血管新生调控因子Lrg1及其他基因和通路。RNA速度分析和伪时间分析显示,低表达Bst1的内皮细胞可能从Procr阳性或Bst1阳性细胞分化而来。此外,高表达Bst1的VESCs候选簇(簇6和簇10)在视网膜+视神经来源的内皮细胞中富集。转录因子Atf3、Irf1和Stat3在簇10中的表达显著高于其他簇,且Atf3结合基序在簇10的转录候选增强子区域富集。
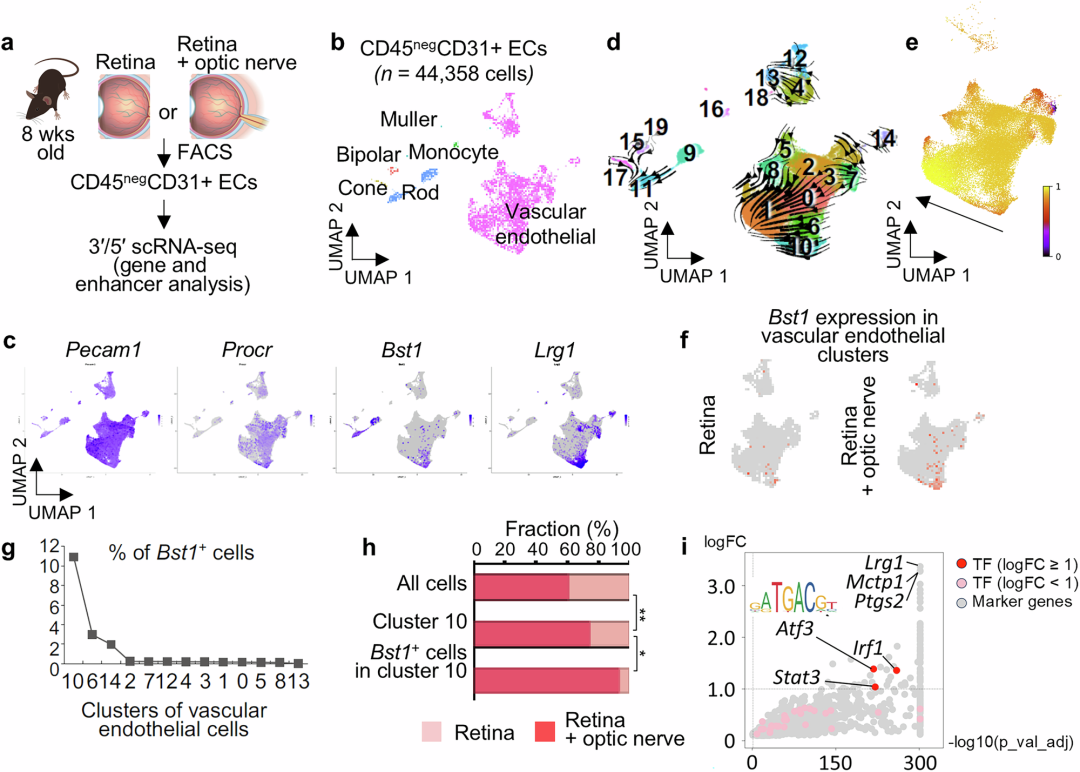
图2:视神经中存在表达祖细胞相关基因的内皮细胞亚群
为定位CD157阳性CD201阳性内皮细胞,将Procr(CD201)-CreERT2小鼠与loxP-tdTomato报告品系杂交。8周龄小鼠单次注射他莫昔芬后2天,tdTomato表达主要集中在视神经血管中;7天后,视网膜中央静脉中出现tdTomato阳性CD31阳性细胞;14天后,视网膜中周血管也出现该类细胞;2个月后,tdTomato阳性细胞主要存在于视神经血管而非视网膜静脉中。这些数据表明,tdTomato标记的细胞发生逆向迁移(逆血流方向迁移),通过毛细血管网从静脉迁移至动脉。
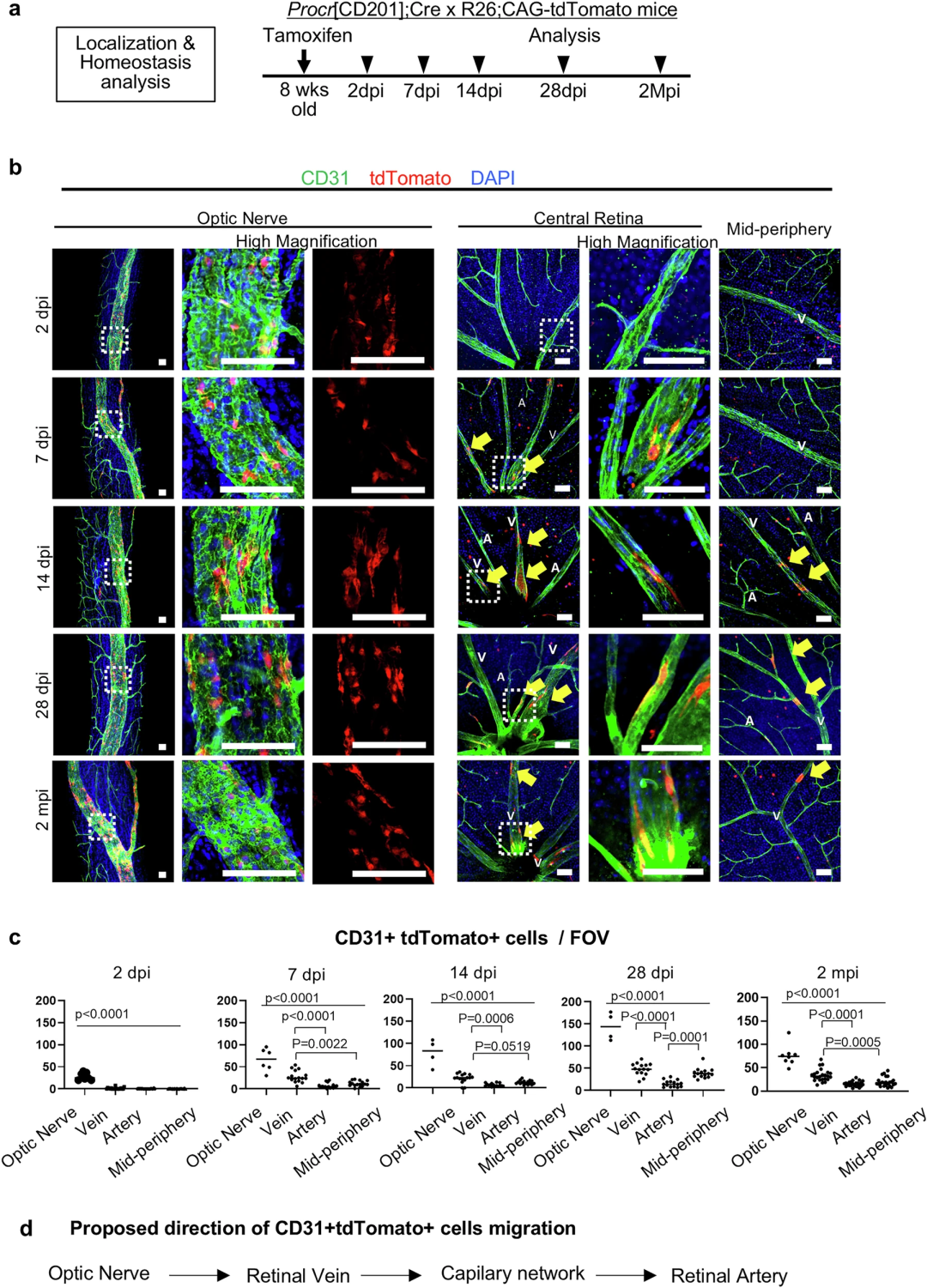
图3:正常状态下,位于视神经内视网膜中央静脉的内皮祖细胞缓慢为视网膜供给内皮细胞
3.3内皮干细胞参与视网膜血管修复
为探究血管修复机制并明确受损血管是否由内皮干细胞/祖细胞形成,本研究采用小鼠血管损伤模型(氧诱导视网膜病变,OIR):小鼠在出生后第7天(P7)置于高氧环境诱导缺血性视网膜病变和血管脱落,P12恢复常氧后,血管新生在P17达到峰值,P30恢复正常。分别收集P12(缺血期)、P17(视网膜病变期)、P25(血管修复期)仅视网膜或视网膜+视神经来源的CD45阴性CD31阳性视网膜内皮细胞(6个损伤样本),并与6个对照样本共同分析。整合12个样本的scRNA-seq数据,鉴定出7个内皮细胞簇,混杂少量感光细胞等。除簇4(主要为感光细胞而非内皮细胞)外,所有簇均高表达脑内皮细胞特异性标志物Pglyrp1。在视网膜+视神经样本中,簇1为内皮干细胞群富集簇,且在P12、P17、P25的视网膜+视神经样本中大量存在。
基于图1n的集落形成实验结果,将视网膜内皮细胞分为四组:Bst1(CD157)阳性Procr(CD201)阳性、Bst1阴性Procr阳性、Bst1阳性Procr阴性、Bst1阴性Procr阴性。分析显示,Bst1阳性Procr阳性内皮细胞在视网膜+视神经样本的簇1中比例更高;且在视网膜血管损伤小鼠的P17和P25样本中,Bst1阴性Procr阳性内皮细胞大量存在。
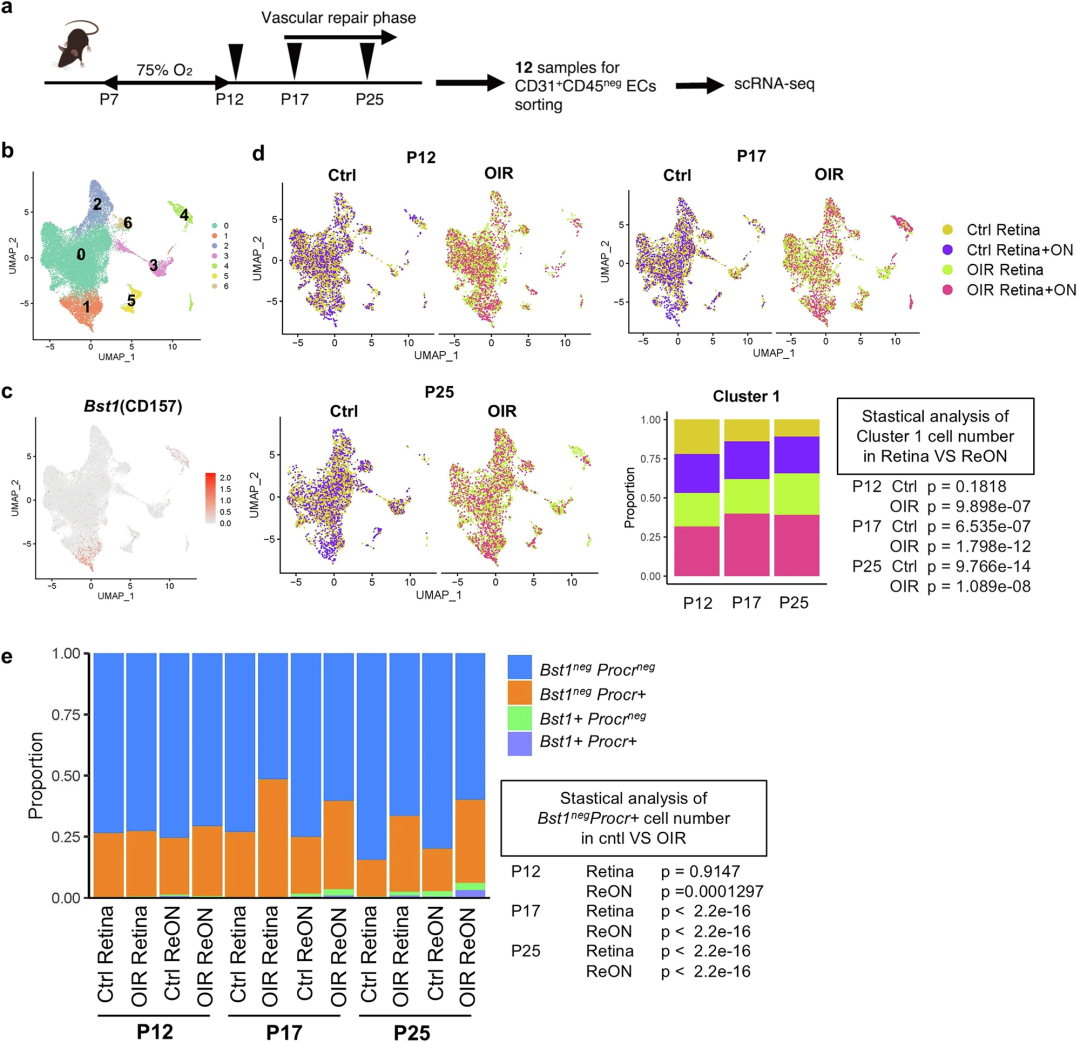
图4:小鼠缺血性视网膜病变损伤后修复过程的单细胞RNA测序提示视网膜血管内皮细胞存在层级结构
3.4视网膜/视神经血管系统中内皮细胞的层级结构
为探究CD201阳性内皮细胞在血管修复中的作用,再次在OIR模型及其生理对照中研究Procr-CreERT2-tdTomato报告小鼠。P12注射他莫昔芬标记VESCs,结果显示:他莫昔芬注射后1天(P13),OIR模型视网膜中仅少量tdTomato标记的CD201阳性内皮细胞,而视神经血管中大量存在;P15时,tdTomato阳性细胞出现在视网膜大静脉的视神经侧,而非外周侧;P17时,视网膜所有大静脉均出现该类细胞;P28时,大部分重建的血管由tdTomato阳性细胞构成。此外,tdTomato阳性细胞重建的血管可改善缺血并具备功能。这些结果表明,驻留于视神经的内皮祖细胞在视网膜血管修复中起关键作用。
FACS分析显示,OIR模型P28(血管修复期)时,视网膜和视神经样本中仅不足5%的CD45阴性CD31阳性内皮细胞为CD201阳性,但超过50%的细胞为CD201阳性细胞的克隆(即tdTomato阳性)。干细胞驻留于微环境的可能原因之一是缺氧,而OIR模型中视网膜存在缺氧,视神经则无缺氧现象。结合体外实验结果(CD157阳性CD201阳性内皮细胞可分化为CD157阴性CD201阳性和CD157阴性CD201阴性内皮细胞),本研究提出层级结构:CD157阳性CD201阳性VESCs位于上游,下游依次为CD157阴性CD201阳性内皮细胞和CD157阴性CD201阴性内皮细胞。
为明确CD201阳性祖细胞在血管修复中的作用,将Procr(CD201)-CreERT2小鼠与诱导型白喉毒素受体(ROSA26iDTR)品系杂交。他莫昔芬和白喉毒素处理后选择性清除Procr阳性细胞,显著增加了P28血管修复期的血管闭塞面积。
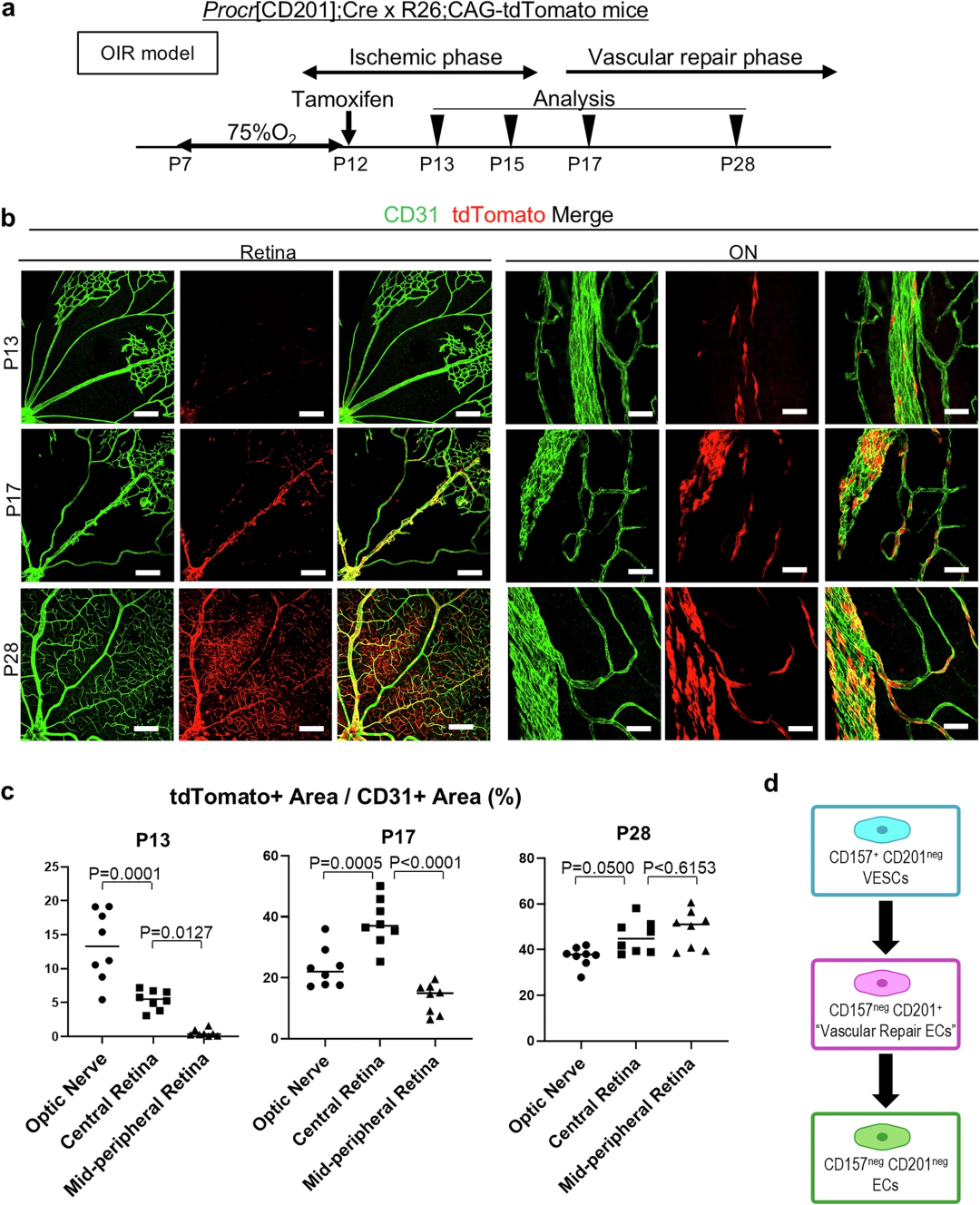
图5:视网膜血管内皮祖细胞亚群的层级分析
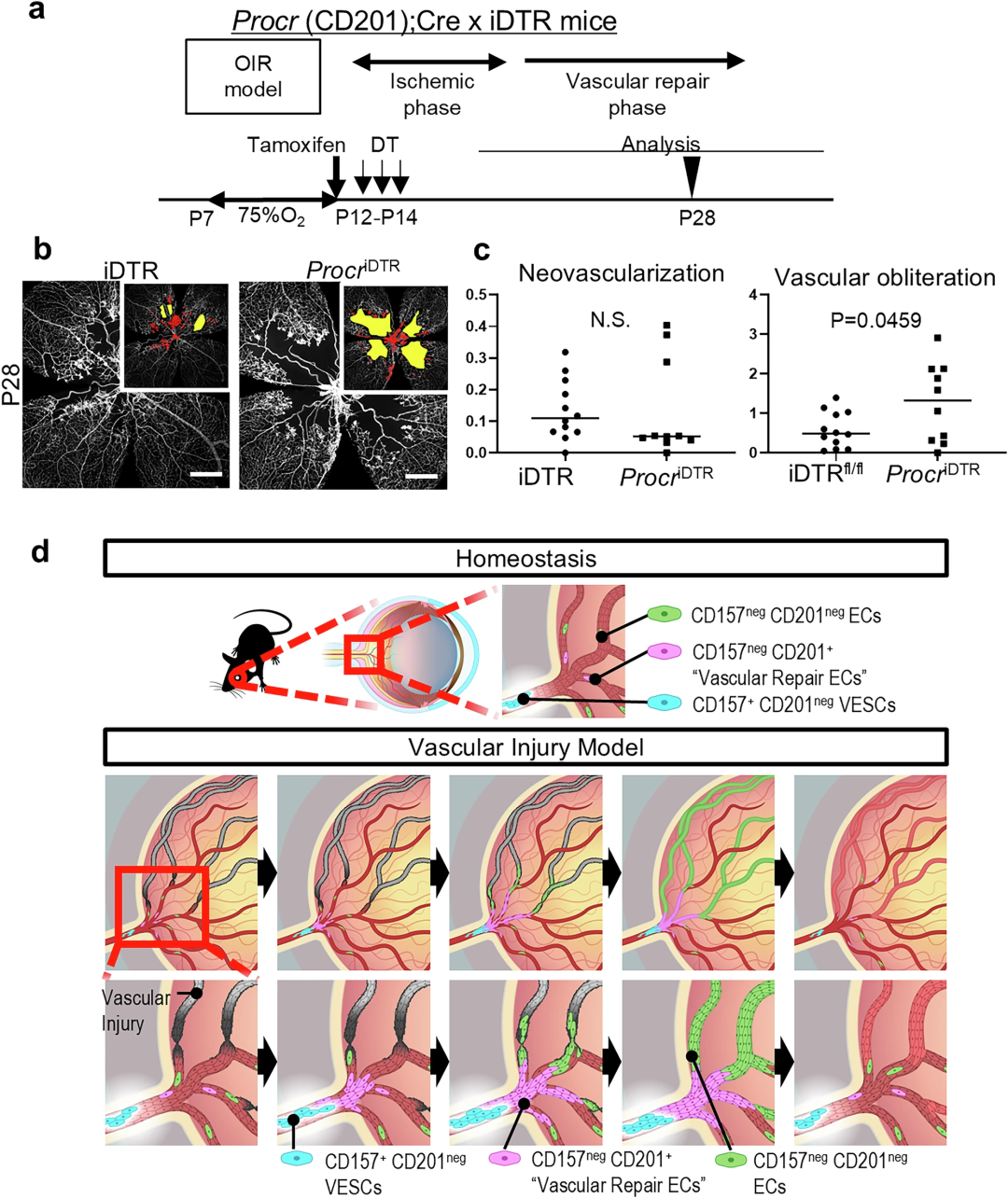
图6:CD201阳性细胞调控氧诱导视网膜病变损伤后的血管修复
3.5内皮祖细胞中的转录因子介导血管修复
为深入探究视网膜VESCs的作用机制,本研究聚焦于候选内皮祖细胞亚群中高表达、且其结合基序在该亚群转录增强子区域富集的转录因子ATF3。构建了内皮祖细胞中条件性敲除ATF3的诱导型细胞特异性小鼠模型(Procr(CD201)-CreErt2/ATF3flox/flox,即ATF3ΔProcr小鼠)。对该小鼠进行OIR实验,结果显示:P12注射他莫昔芬后,P17和P21的视网膜血管闭塞面积显著增大;而P7注射他莫昔芬后,P12的血管闭塞面积无明显变化。
四、讨论
血管生物学领域长期存在的核心问题之一是:负责组织稳态和重塑的内皮细胞究竟来源于何处?本研究通过scRNA-seq、集落形成实验、谱系示踪和基因靶向分析等多方面证据,证实表达干细胞标志物的内皮细胞大量存在于视神经中,并为视网膜供给内皮细胞。本研究提出的细胞层级模型具有两大特征:(1)稳态条件下,视神经富集的祖细胞缓慢为视网膜供给内皮细胞;(2)损伤后,CD201阳性CD157阴性内皮细胞激活并参与血管修复。
与该模型一致,选择性清除Procr(CD201)阳性谱系(Procr-creERT2;ROSA26iDTR)后,修复期(P28)的血管闭塞增加,但病理性血管簇未减少。这与Procr-CreERT2-tdTomato报告小鼠中tdTomato阳性细胞在病理性血管簇中稀疏、而在视网膜大血管中富集的观察结果相符。此外,泛内皮ATF3敲除也得到相同结果(无血管区扩大,病理性血管簇不变)。这些发现支持Procr谱系细胞在应激状态下维持和重建生理性毛细血管丛,而非直接驱动病理性血管簇形成。
尽管本研究数据支持视神经富集祖细胞的主要贡献,但不能排除其他来源的参与;例如,骨髓来源细胞可能在炎症或缺血条件下协同作用。未来研究应量化视神经与其他来源的相对贡献。
从解剖和发育角度,视网膜常被视为中枢神经系统的延伸。本研究发现的视神经干细胞微环境为视网膜血管供给内皮细胞,进一步印证了这一观点。视神经中视网膜内皮干细胞的鉴定,为开发通过诱导内皮干细胞修复视网膜的治疗策略治疗视网膜疾病提供了可能。例如,在增殖性糖尿病视网膜病变(糖尿病视网膜病变的最晚期)中,新生血管起源于视网膜静脉和毛细血管,但这些新生血管结构脆弱,显著增加眼内出血和/或视网膜脱离的风险。若能从视神经干细胞库来源的内皮细胞生成更正常的血管,或可降低此类风险。
本文相关文献:Sakimoto,S.,Takigawa,T.,Oguchi,A.et al.Endothelial stem cells of the retinal vasculature reside in the optic nerve.Nat Commun 17,606(2026).https://doi.org/10.1038/s41467-025-68201-6








